আমাদের চারপাশে অসংখ্য জিনিস আছে। যেমনঃ বাড়ি-ঘর, গাছ-পালা, মাটি, পানি, কাঁচ, লোহা প্রভৃতি। এর সব কিছুই পদার্থের তৈরী। সহজভাবে বলতে এই বিশ্বব্রহ্মাণ্ডের সবই পদার্থের তৈরী। তাহলে পদার্থ কি?
সাধারণত যা কিছুর ভর আছে তাই পদার্থ। এই ভর থাকায় পদার্থের কিছু মৌলিক বৈশিষ্টের সৃষ্টি হয়। সেগুলোকে উপরের সংজ্ঞার সাথে জুড়ে দিলেই পাওয়া যায় পদার্থের সর্বজন গৃহীত সংজ্ঞা। তা হচ্ছে-
“যার ভর আছে, জায়গা দখল করে ও জড়তা আছে- অর্থাৎ বল প্রয়োগে বাধার সৃষ্টি করে তাকে পদার্থ বলে।”
পদার্থকে ভৌত অবস্থার এবং রাসায়নিক গঠনের উপর ভিত্তি করে বিভিন্ন ভাগে ভাগ করা যায়।
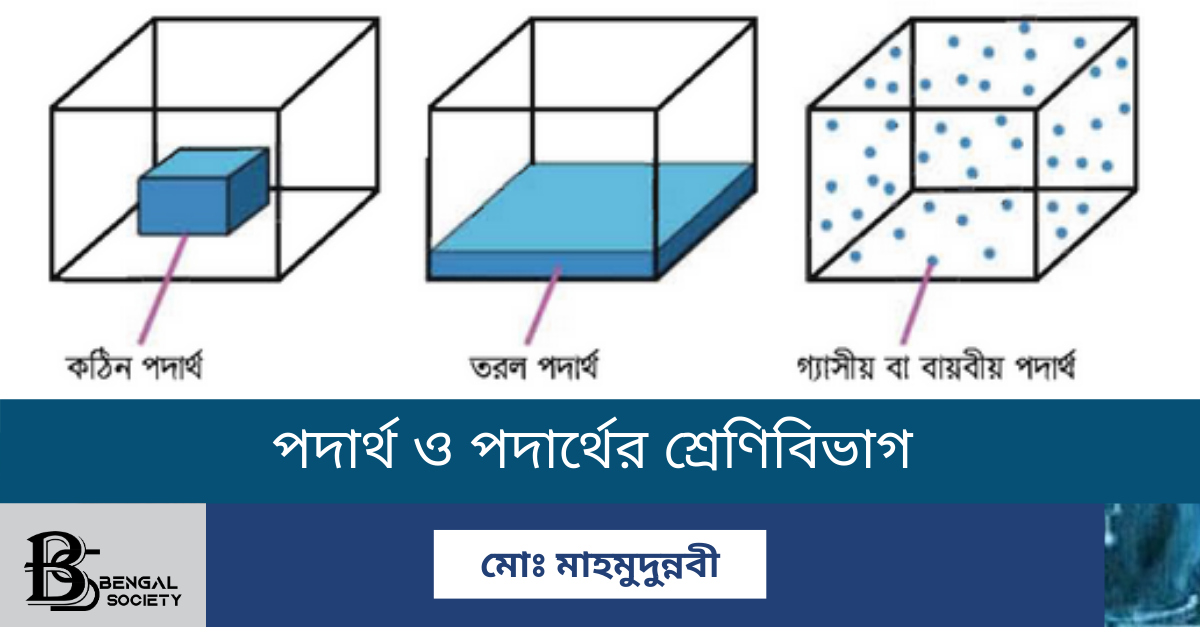
সাধারণ পরিবেশে ভৌত অবস্থাভেদে পদার্থ আমরা প্রধানত তিনটি অবস্থায় পাই। যথা- কঠিন, তরল এবং বায়বীয়। নিচে এদের সম্পর্কে বিস্তারিত লেখা হলো।
১। কঠিন পদার্থ- যে পদার্থের নির্দিষ্ট আকার এবং আয়তন আছে তাকে কঠিন পদার্থ বলে। কঠিন পদার্থে কণা বা অণুগুলোর আন্তঃআণবিক শক্তি খুব বেশি থাকে এবং আন্তঃআণবিক দূরত্বও অপেক্ষাকৃত অন্য দুই অবস্থার থেকে অনেক কম।
২। তরল পদার্থ- যে ভৌত অবস্থায় পদার্থ নির্দিষ্ট আয়তন প্রদর্শন করে কিন্তু নির্দিষ্ট আকার থাকে না। যে পাত্রে রাখা হয় তার আকার ধারণ করে, তাকে তরল পদার্থ বলে। এই পদার্থের অণুগুলো পরস্পরের সাথে শিথিল আন্তঃআণবিক শক্তির মাধ্যমে আবদ্ধ থাকে। তাই তারা নির্দিষ্ট আকার বা আকৃতি প্রদর্শন করে না। যেমনঃ পানি, কেরোসিন, মধু, গ্লিসারিন ইত্যাদি।
পানিকে আমরা যদি বোতলে রাখি তবে তা বোতলের মতই আকার নেয়, যদি বালতিতে রাখি তবে নেয় বালতির আকার। সকল তরলের জন্যই এই বৈশিষ্ট্য একই।
৩। বায়বীয় পদার্থ- বায়বীয় বা গ্যাসীয় পদার্থে আন্তঃআণবিক শক্তি প্রায় থাকে না বললেই চলে। থাকলেও তা খুবই দূর্বল। তাই এর অণুগুলো প্রায় স্বাধীন ভাবে এবং দ্রুত নড়াচড়া করতে পারে। এজন্য বায়বীয় পদার্থের নির্দিষ্ট আকার তো নেইই, সেইসাথে এর কোন নির্দিষ্ট আয়তনও থাকে না। যে পাত্রেই রাখা হোক না কেন, সেই পাত্রেরই পুরো আয়তন জুড়ে বিরাজ করে। সুতরাং বলা যায় যে-
যে ভৌত অবস্থায় কোন পদার্থের নির্দিষ্ট আকার বা আয়তন থাকে না তাকেই বায়বীয় পদার্থ বলে। যেমনঃ অক্সিজেন, নাইট্রোজেন বা কার্বন-ডাই- অক্সাইড ইত্যাদি।
এখানে উল্লেখ্য যে, পদার্থের ভৌত অবস্থা তাপ এবং চাপের উপর নির্ভর করে। তাই তাপ বা চাপ প্রয়োগ অথবা অপসারণের মাধ্যমে প্রতিটি পদার্থকে এক অবস্থা থেকে অন্য অবস্থায় রূপান্তরিত করা যায়। যেমনঃ সাধারণ তাপমাত্রায় পানি তরল হিসেবে থাকে। তাকে আমরা রেফ্রিজারেটরে ঠান্ডা করলে বরফ পাই- যা কঠিন পদার্থ। আবার চুলায় রেখে ফুটালে তা গ্যাস বা বায়বীয় আকার ধারণ করে। পদার্থের এই পরিবর্তন সচরাচর কঠিন থেকে তরল এবং তরল থেকে বায়বীয়- এভাবে অথবা তার বিপরীত ভাবে হয়। কিন্তু কিছু কিছু পদার্থ আছে যারা কঠিন থেকে তরল না হয়ে সরাসরি বায়বীয় পদার্থে পরিণত হয়। এদের উদ্বায়ী পদার্থ বলে। যেমনঃ ন্যাপথলিন, কর্পুর।
আবার কঠিন, তরল বা বায়বীয় অবস্থা ছাড়াও পদার্থ আরো দুটি ভৌত অবস্থা আছে যদিও সাধারণভাবে সেগুলোকে আমরা দেখতে পাই না। সেগুলোর একটা প্লাজমা, সহজ করে বললে, উচ্চ তাপমাত্রায় পদার্থের গ্যাসীয় অবস্থা। অগ্নি শিখার উপরের গ্যাসীয় পদার্থ হল প্লাজমা, যার পরমাণু থেকে এক বা একাধিক ইলেকট্রন বিচ্ছিন্ন হয়ে গিয়েছে। সূর্য থেকে ধেয়ে আসা কণিকা প্রবাহ আসলে প্লাজমা প্রবাহ। বিশ্বব্রহ্মান্ডের সর্বত্র রয়েছে প্লাজমা। আরেকটি, বোস-আইনস্টাইন কনডেনসেট। অদ্ভুত এর বৈশিষ্ট, এর ধর্ম ; এটি কঠিন পদার্থও নয়, তরল পদার্থও নয়, গ্যাসীয় বা প্লাজমা ও নয়, একেবারে আলাদা। বিশ্বব্রহ্মান্ডের কোথাও বোস-আইনস্টাইন কনডেনসেট এর অস্তিত্ব নেই, পৃথিবীতে মানুষের তৈরি গবেষণাগার ছাড়া। কারণ তার জন্য প্রয়োজন অকল্পনীয় শৈত্য তথা নিম্ন তাপমাত্রা। একশো সত্তর (১৭০) ন্যানো-কেলভিন তাপমাত্রা তথা এক কেলভিন (সহজ করে বললে এক সেন্টিগ্রেড) তাপমাত্রার একশো কোটি ভাগের একশো সত্তর ভাগ। একই সঙ্গে পৃথিবীর সমুদ্রতলের বাতাসের চাইতে এক লক্ষগুণ পাতলা আবদ্ধ গ্যাস।
রসায়নবিদ্যায় পদার্থকে প্রধান দুইটি শ্রেণিতে ভাগ করা হয়। যথাঃ মৌলিক পদার্থ এবং যৌগিক পদার্থ।
১। মৌলিক পদার্থঃ যে পদার্থকে ক্ষুদ্র ক্ষুদ্র অংশে ভাগ করলে ওই পদার্থ ছাড়া অন্য কোনো পদার্থ পাওয়া যায় না, তা-ই মৌলিক পদার্থ।যে পদার্থকে রাসায়নিক পদ্ধতিতে বিভাজিত করে দুই বা ততোধিক ভিন্ন ধর্মবিশিষ্ট পদার্থে বিশ্লিষ্ট করা যায় না, অর্থাৎ যে পদার্থ হতে সাধারণভাবে সেই পদার্থ ব্যতীত অন্য কোন নূতন পদার্থ পাওয়া যায় না, তাকে মৌল বা মৌলিক পদার্থ বলে। যেমনঃ হাইড্রোজেন (H2), সোডিয়াম (Na)। হাইড্রোজেনকে যত ভাগে ভাগ করা হোক- হাইড্রোজেনই পাওয়া যাবে। একইভাবে সোডিয়ামকে ভাগ করলেও শুধু সোডিয়ামই পাওয়া যায়।
২। যৌগিক পদার্থঃ যে পদার্থ থেকে দুই বা ততোধিক সম্পূর্ণ ভিন্ন ধর্মবিশিষ্ট মৌলিক পদার্থ পাওয়া যায়, সেই পদার্থকে যৌগ বা যৌগিক পদার্থ বলে। যেমনঃ যেমন : খাবার লবণ বা সোডিয়াম ক্লোরাইড (NaCl)
এখানে সোডিয়াম ক্লোরাইডকে ভাগ করলে সোডিয়াম (Na) ও ক্লোরিন (Cl) পাওয়া যাবে।
এছাড়াও রসায়নবিদ্যায় মিশ্রণ বা মিশ্র পদার্থ হিসেবে পদার্থের একটি রূপ প্রকাশ করা হয়। দুই বা তার অধিক মৌলিক অথবা যৌগিক পদার্থের ভৌত সমবায়ে গঠিত পদার্থকে বোঝায়। মিশ্র পদার্থের পদার্থগুলি কোন রাসায়নিক বন্ধন বা অন্যকোন রাসায়নিক পরিবর্তন ছাড়াই অর্থাৎ যার যার গঠন ও ধর্ম বজায় রেখে যান্ত্রিকভাবে মিশ্রিত থাকে। যেমনঃ বাতাস- এতে অক্সিজেন, নাইট্রোজেন, কার্বন-ডাই-অক্সাইড সহ আরো অনেক পদার্থ নিজ নিজ গুণ বজায় রেখে বর্তমান।
রেফারেন্স-
লিখেছেন,
মোঃ মাহমুদুন্নবী